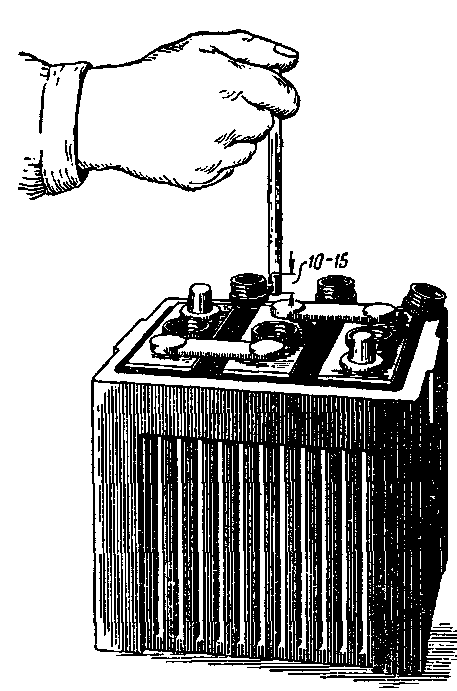
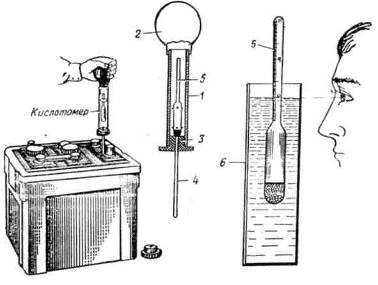
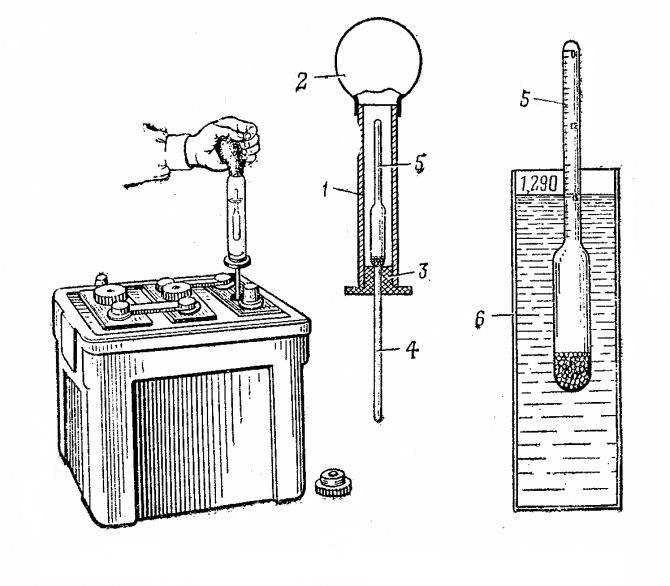
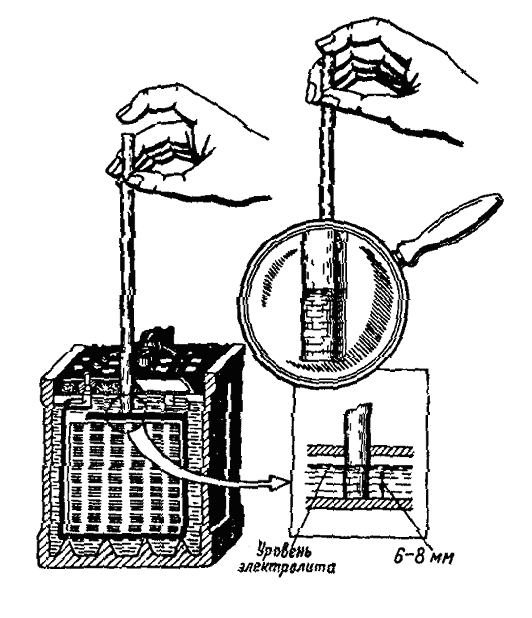
Процессы, происходящие в АКБ с участием электролита
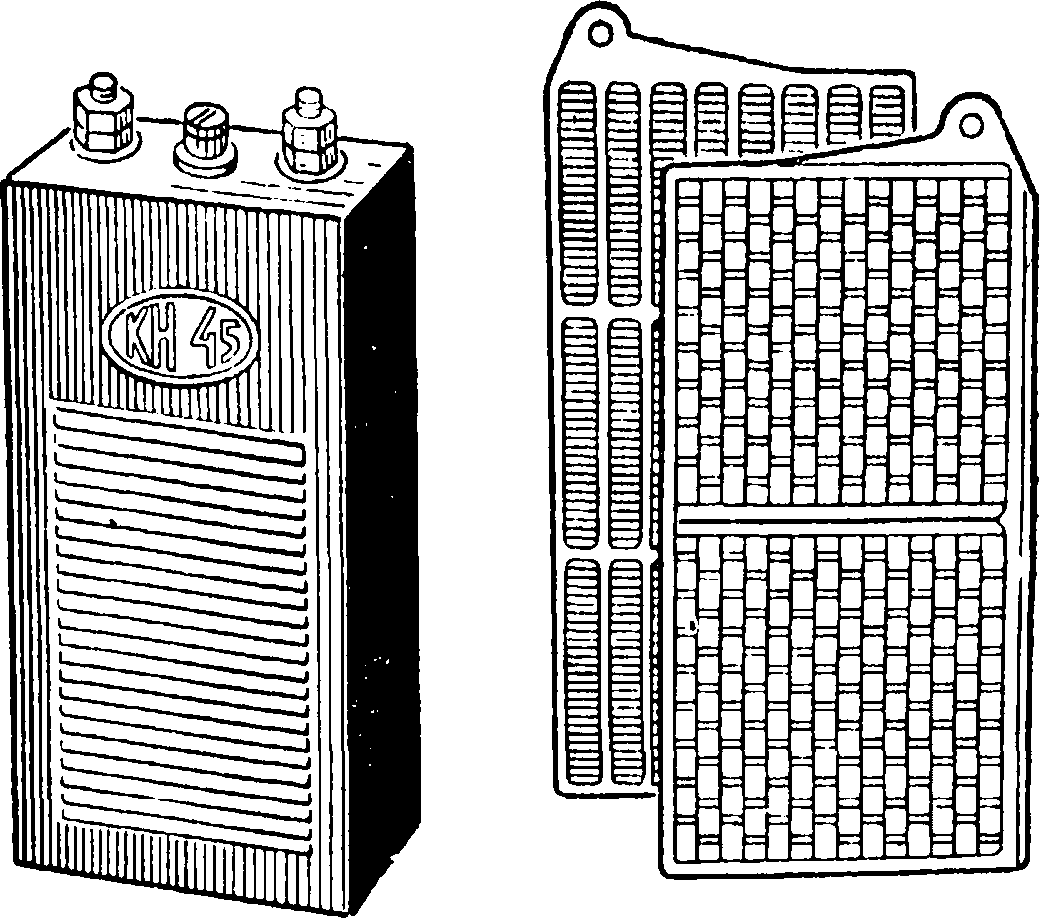
Работа свинцово-кислотного автомобильного аккумулятора основывается на электрохимических процессах, которые протекают с участием электролита. Аккумулятор автомобиля состоит из положительных и отрицательных пластин, погруженных в водный раствор серной кислоты. Положительные и отрицательные пластины имеют токоотводящие решётки из свинца с различными добавками в зависимости от типа аккумулятора. На решётках положительных электродов нанесён красновато-коричневый диоксид свинца (PbO2). На отрицательных электродах — сероватый порошок свинца (Pb). Электрические характеристики аккумулятора напрямую зависят от плотности электролита. Для понимания назначения электролита нужно рассмотреть основные процессы, происходящие в аккумуляторе автомобиля.
При разряде аккумулятор на положительном электроде (аноде) идёт следующая реакция:
PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O
На отрицательном электроде (катоде) протекает такой процесс:
Pb + SO42− − 2e− ->PbSO4
При заряде АКБ эти реакции протекают в обратном направлении. Электролит в свинцово-кислотном автомобильном аккумуляторе имеет разную плотность в зависимости от степени заряженности АКБ. Как уже говорилось выше, концентрированная кислота аккумуляторного сорта имеет плотность 1,835 гр/см3. Плотность электролита на заряженном аккумуляторе лежит в диапазоне 1,127─1,300 гр/см3. При разрядке аккумулятора автомобиля в результате электрохимической реакции из электролита расходуется серная кислота и его плотность падает. Пока через батарею проходит ток разряда кислота рядом с электродами расходуется в результате вышеописанной реакции. Идёт диффузия H2SO4 из объёма к электродам. Таким образом, поддерживается напряжение на выводах аккумулятора. В начале разрядки процесс диффузии кислоты в электроды. Это объясняется тем, что в активной массе электродов поры ещё не забиты сульфатом. По мере того, как на них образуется слой сульфата и забивает поры, процесс диффузии притормаживается. В теории процесс разряда может идти до того момента, пока электролит не превратится в воду. Но на практике разряд идёт до тех пор, пока плотность не опуститься до значения 1,15 гр/см3. К моменту падения плотности до 1,15 гр/см3 выделяется столько сульфата свинца, что его хватило для закупоривания активной массы пластин. По плотности электролита можно судить о степени заряженности АКБ. Для этого можно использовать таблицу, представленную ниже.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
| 1,11 | 11,7 | 8,4 | -7 | |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
Полностью заряженный элемент АКБ автомобиля выдаёт напряжение 2,5─2,7 вольт без нагрузки на выводах. При подключении нагрузки напряжение проседает до 2,1 вольта за несколько минут. За это время успевает сформироваться слой PbSO4 на поверхности отрицательных электродов. То есть, напряжение одного элемента на подключённой к автомобилю АКБ составляет примерно 2,15 вольта. Если разряжать аккумулятор автомобиля небольшим током (10 процентов от номинальной ёмкости), то через час разрядки напряжение элемента снижается до 2 вольт. Это происходит из-за того, что в этом момент быстро формируется большое количество PbSO4, который забивает поры активной массы. В результате растёт внутреннее сопротивление элементов АКБ и падает концентрация электролита. Через некоторое время процесс разрядки выходит на прямую (см. график).
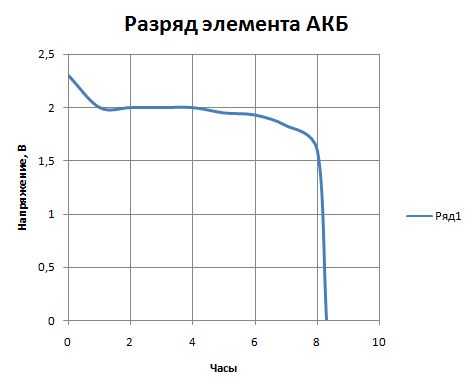
График разрядки аккумулятора Эта прямая соответствует балансу плотностью электролита около электродов и в остальном объёме. Постепенно кислота поступает из объёма к электродам и вступает в реакцию с выделением сульфата свинца. Плотность электролита постепенно снижается, а напряжение падает медленнее, чем на начальной стадии. И на конечной стадии, когда активная масса блокируется образовавшимся сульфатом свинца, реакция замедляется и напряжение быстро падает.
Требования безопасности при самостоятельном приготовлении
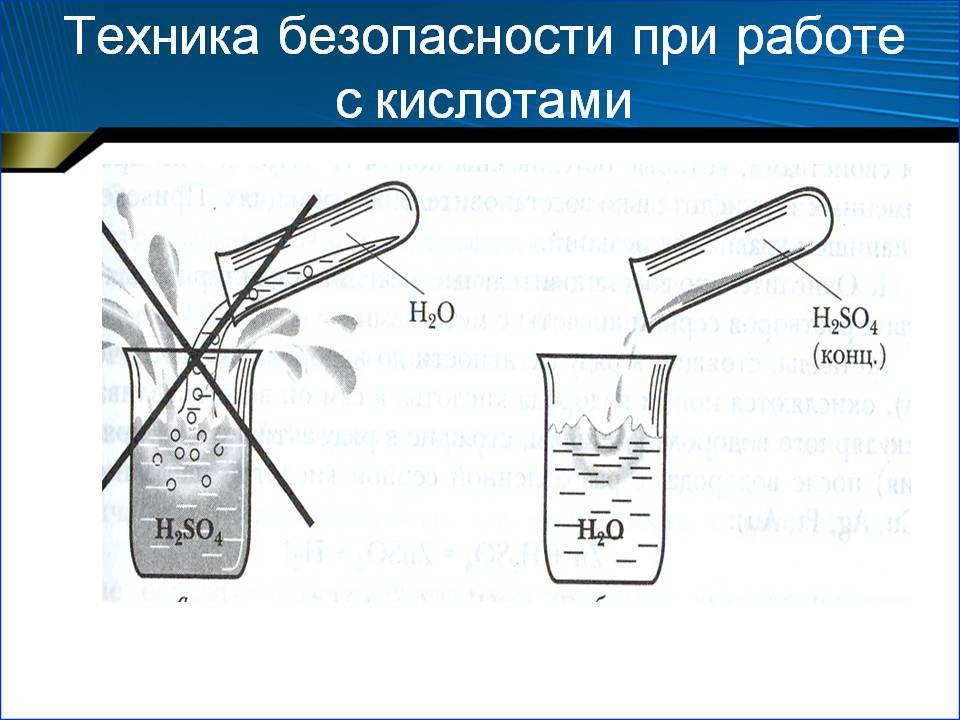
Если вы решили сделать электролит для заправки своей свинцовой аккумуляторной батареи в домашних условиях, то крайне важно соблюдать технику безопасности. Согласно этим правилам, состав приготовляется при выполнении следующих условий:
Согласно этим правилам, состав приготовляется при выполнении следующих условий:
Средства защиты. Они нужны для защиты глаз, кожи и органов дыхания
Важно использовать такие средства защиты, которые будут устойчивыми к агрессивным веществам. Потому на глаза надевают очки, на руки резиновые перчатки
Желательно резиновые сапоги на ноги и защитный фартук на тело.
Нейтрализатор. Если кислота случайно разольётся, её следует засыпать нейтрализующим составом. Как известно, кислота нейтрализуется щёлочью. Потому наготове следует держать водный раствор на основе кальцинированной соды, либо нашатырный спирт. Обычно пищевая сода есть в каждом доме.
Ёмкость для смешивания. Перемешивать между собой ингредиенты следует только в ёмкости из стекла или пластика. Материал должно быть устойчивым к агрессивным веществам. Если это щелочной раствор, тогда берите стальную или пластиковую тару. Ни один другой материал для таких целей не подходит.
Проветриваемое помещение. Оптимально делать это на улице под навесом. Либо выбирать помещение с хорошей вентиляцией. Выделяющие кислотные и щелочные пары могут нанести вред здоровью, проникая в организм через дыхательные пути.
Постепенное добавление. При приготовлении смеси своими руками кислоту постепенно заливают воду небольшими порциями. Жидкость требуется регулярно помешивать при этом, и стараться не останавливаться.
Соблюдение таких требований и правил убережёт вас от ошибок, сохранит здоровье, а также позволит успешно перезалить аккумуляторную батарею.
Основные ошибки конструирования самодельных зарядных устройств
Ошибки в конструировании связаны с тем, что мастера стремятся сделать схему проще. Приборы нередко состоят только из понижающего трансформатора и выпрямителя без устройств контроля и защиты.
Поэтому в работе с такими упрощенными самодельными ЗУ необходимо придерживаться следующих правил:
- Постоянно контролировать процесс, не допускать перезаряда. Если нет возможности установить измерительные приборы в устройство, пользуются отдельным мультиметром.
- Не оставлять без присмотра. Мастера нередко отказываются от установки устройств, которые при превышении допустимых параметров автоматически отключают зарядку. Это иногда оборачивается большими неприятностями при бесконтрольном процессе.
- Правильно подсоединять минус и плюс, чтобы не повредить пластины АКБ. У заводских приборов есть встроенная защита от такой ошибки.
- Подсоединять к аккумулятору только что выключенное устройство.
- Сборку прибора следует проводить аккуратно: на входе опасные для жизни 220 В. Кроме того, ошибки в монтаже способны при включении вывести АКБ из строя.

Если придерживаться этих рекомендаций, можно делать подзарядку даже самым простым прибором, не опасаясь неприятностей.
Щелочные электролиты
Для их создания применяют литий и калий, они обои являются едкими.
Едкий калий или сокращенно КОН является белым, твердым и отлично растворимым в H2O. Когда идет растворение выделяется тепло. По гост стандарту это вещество выпускается четырех сортов:
- Высший.
- А
- Б тип.
- Реактивные.
В первом варианте едкого калия содержится до 96%. Во втором типе «А» до 92%. В третьем сорте Б его 88%. Четвертый вариант имеет мало примесей чем технический.
Когда создание электролита планируется из лития и калия первым делом необходимо растворить калий, а потом добавить литий. Все это делается из расчета 10-20 грамм на 1 литр электролита. После этого его нужно оставить на 15-20 ч. Это нужно для того чтобы температура упала и примеси выпали в осадок. Перед оставлением его раствор нужно закрыть хорошо крышкой.
Затем получившийся жидкий раствор следует слить в чистую посуду. Далее проверить уровень плотности ареометром. Если необходимо плотность доводят до нормы. После этого добавляют щелочь и воду. Так же можно добавить готовый концентрированный электролит.
Какая плотность нужна для вашего аккумулятора? Это информацию можно узнать в его технической документации. Если документы не содержат какие-то критические советы, то можно использовать электролит 1,19-1,21 г/см3 при t 15 градусов. Так же в нем должно быть 10-20 г/л Li.
Следует знать, что жидкость с такими характеристиками лучше использовать при t не ниже 20 градусов. При низких температурах подойдет плотность 1,25—1,27 г /см3. Но без использования едкого Li.
Чтобы реанимировать железоникелевые и щелочные кадмий-никелевые АКБ используют электролит на основе лития и калия плотностью 1,255—1,279 г/см3. К этому всему еще нужно добавить 69 грамм едкого Li на 1 литр электролита.
Для удобства приготовления воспользуйтесь таблицей.
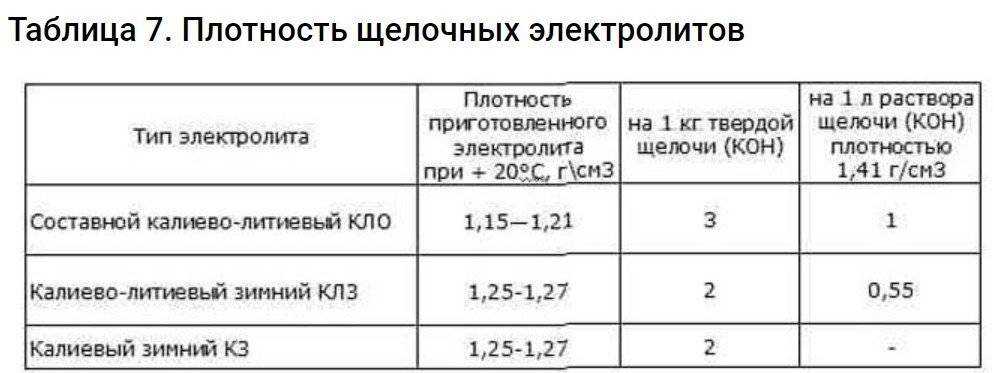
Срок годности электролита
Он может храниться бесконечно долгое время. Чтобы не было осадков уберите его из-под солнечных лучей. Так же старайтесь чтобы не было скачков температуры. Электролит находящийся в АКБ в действительности не известно сколько прослужит. Так как на него влияют многие факторы.
Виды электролита
Электролиты бывают двух основных видов:
- Кислотный.
- Щелочной.
Кислотные смеси с дистиллированной водой применяются в основном в аккумуляторах, применяемых для запуска двигателя автомобиля. Такие вещества можно приобрести в специализированных магазинах либо приготовить самостоятельно. На заводе такие смеси делают по ГОСТу, в домашних условиях также можно довольно точно соблюсти необходимые пропорции при смешивании кислоты с водой.
Щелочная смесь может быть приготовлена с использованием различных активных веществ, но наиболее часто применяется кальциево-литиевая основа, которая разводится необходимым количеством дистиллированной воды.

Конструктивные особенности
Аккумулятор состоит из гидроокиси никеля, а также некоторых иных элементов. Из-за того, что в составе имеется графит, это оказывает положительное влияние на электрическую проводимость. Различные примеси осуществляют нормальную работоспособность и стабильность аппарата.
Чтобы подготовить отрицательный элемент, используют металлический сплав кадмия, никеля и определённого порошка. В каждом случае АКБ будет иметь свои особенности. Электролит включает в себя моногидрат лития. Благодаря этому элементу обеспечивается долгая деятельность агрегата.
В состав батареи входят следующие компоненты:
- Изоляционный слой, изготовленный из качественного сырья.
- Прокладка из пластика, которая дополняется специальным клапаном.
- Корпус.
- Выводы и контакты.
Это все основные элементы щелочного аккумулятора. Все компоненты выполнены из надёжных материалов, а потому проблем с работой не возникает.
Химические процессы
Принцип работы очень простой. Когда происходит полная разрядка, гидроокись никеля начинает взаимодействовать с щелочным раствором. В результате образовывается гидрат закиси никеля. На выводе с минусом будет происходить очень похожий процесс. Начинают формироваться определённые элементы.
Когда идёт процесс зарядки, проходит обратная реакция. В результате получится гидроокись никеля, которая восстанавливает минусовый электрод.
От кислотных агрегатов щелочный отличается тем, что субстанция, выработанная в ходе химической реакции, не будет растворяться. Она также не в состоянии реагировать с похожими компонентами. Если говорить проще — принцип действия источника питания зависит от определённых канонов.
Этот источник питания необходимо полностью заряжать. Если произойдёт неполный заряд батареи, то период использования сильно сократится. Но при этом нельзя перезаряжать устройство, поскольку это приведёт к сильному перегреву. В результате электроды просто разрушатся.
Замена электролита
Замену электролита необходимо производить через 100 и 150 циклов. До смены потребуется полностью разрядить АКБ и проследить, чтобы номинальный ток составлял до 1 В.
Электролит нужно предельно тщательно удалять из батареи. Чтобы осадок не остался, необходимо встряхнуть аккумулятор во время чистки.
После того, как электролит будет вылит, нужно хорошо промыть агрегат дистиллированной водой. А также можно применять раствор из щёлочи.
Когда процесс очистки завершится, можно сразу же залить новый электролит. После его потребуется оставить в залитом состоянии примерно на 3 часа. Только тогда можно проверить плотность нового вещества.
Гальваника
Существует два способа:
- Готовят три раствора: 60 г фосфата натрия с 700 г воды; 2,5 г хлорида золота и 150 г воды; 1 г цианида калия и 10 г сульфата натрия со 150 г воды. Первые два раствора смешивают, третий добавляют последним. Температура — 50-60 градусов. Анод — из платины. При истощении электролитного раствора добавляют хлорид золота.
- Ванна по Зельми: по 1 г гексацианоферрата калия (желтого) и карбоната натрия смешать с 30 г воды, нагреть в чашке из фарфора. Добавить в смесь осажденное нашатырным спиртом золото. Кипятить в течение 10-12 минут. При испарении воды ее добавляют, пропускают через раствор ток элемента Даниеля. Время воздействия — 15-16 часов.
Способы позолоты в домашних условиях трудоемки и не всегда доступны. Предпочтителен метод химического золочения или натирания.
Готовим электролит для аккумуляторов в домашних условиях самостоятельно
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации.
Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Электролит — электропроводящий раствор, содержащий в своём составе дистиллированную воду и серную кислоту, едкий калий или натрий в зависимости от типа источника питания. Этот показатель кислотности напрямую зависит от необходимой плотности электролита. Изначально средняя концентрация этого раствора в автомобильном аккумуляторе — около 40% в зависимости от температуры и климата, в которых используется источник питания.
Во время эксплуатации концентрация кислоты падает до 10–20%, что сказывается на работоспособности АКБ.
Вместе с тем стоит понимать, что аккумуляторная серная составляющая — наичистейшая жидкость, которая на 93% состоит непосредственно из кислоты остальные 7% — примеси. На территории России производство этого химиката строго регламентировано — продукция должна соответствовать требованиям ГОСТ. Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов.
В зависимости от состава принято выделять щелочной и кислотный электролиты.
Изготовляем электролит своими руками
На сегодняшний день рынок аккумуляторных батарей предлагает автолюбителям массу различных вариантов аккумуляторов. Главный критерий, по которому выбираются батареи – долгий срок службы электролита внутри. Можно приобрести сухозаряженные АКБ и потом сделать электролит самостоятельно, либо купить уже готовый вариант, залитый в заводских условиях.
Рекомендуем прочесть: Если сотруник принять на в приказе какую запралату нудно отображать
После покупки обслуживание можно делать либо своими руками, либо в специальных сервисах.
Перед тем как начинать приготовление электролита, нужно подготовить все необходимые для этого вещи.
Вам потребуются такие элементы процесса:
Специальная эбонитовая или керамическая посуда, объемом не менее 4 литров
Важно, чтобы посуда была стойкая к кислоте.
Инструмент для размешивания щелочных материалов. Так как делать это вы будете своими руками, то инструмент также должен тоже быть кислотоустойчивым.
Дистиллированная вода.
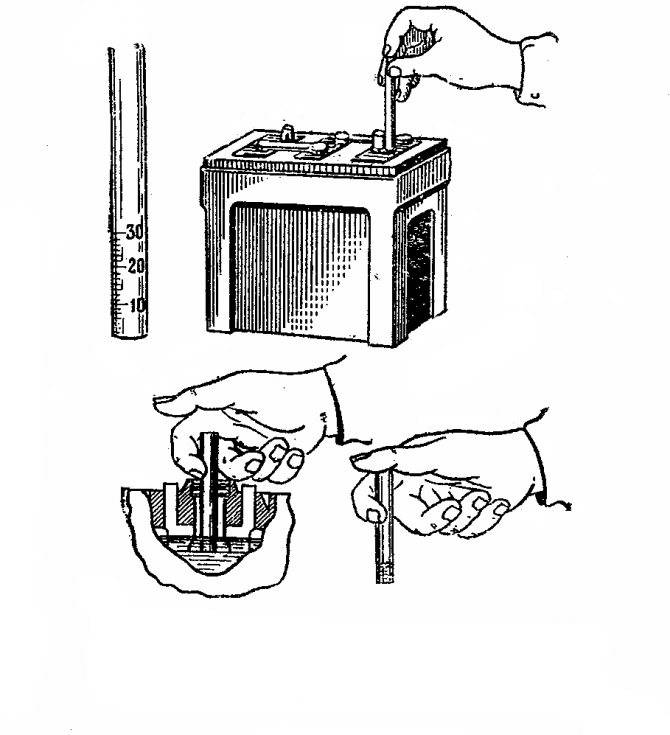
Ареометр.
Серная кислота
Обязательно требуется использовать специальную аккумуляторную серную кислоту.
Приготовление сопровождается соблюдением техники безопасности, вам потребуются:
- Резиновые перчатки.
- Халат или плотный фартук.
- Защитные очки для глаз.
- Нашатырная и борная кислота.
Только имея все необходимое, допускается своими руками готовить электролит.
По правилам техники безопасности, сделать электролит можно будет только после того, как выполняющий все операции человек будет должным образом защищен всеми доступными средствами защиты.
Перед тем как приступать к делу, еще раз в голове прокрутите последовательность действий, чтобы ничего не перепутать, проверьте под рукой ли ареометр. Итак, начинать нужно с промывки всей используемой посуды дистиллированной водой, а после этого посуда обязательно должна высохнуть. Также нужно сказать, что между приготовлением электролита с нуля и доливкой в аккумулятор есть существенная разница.
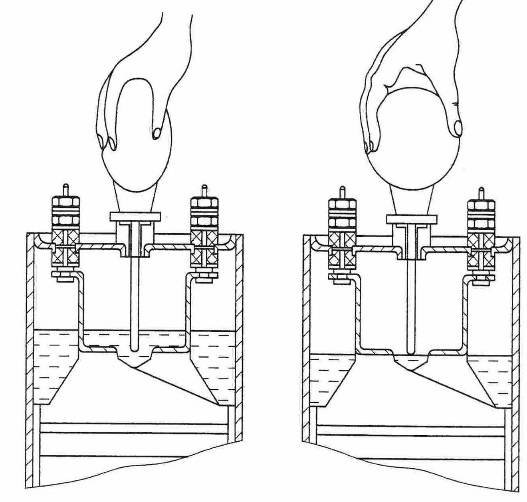
Когда у вас ареометр показал упавшую плотность в АКБ, то вы должны долить внутрь только воды, ни в коем случае не кислоты. Когда же вы готовите электролит с нуля, то в емкость сперва наливается вода, а потом кислота.
Все дело в том, что серная кислота продается концентрированная, из расчета на емкость стандартных видов аккумуляторов. При соприкосновении с водой начинается химическая реакция, при этом если перепутать ингредиенты, то реакция начнет сопровождаться всплесками и значительным увеличением температуры.
Во время изготовления жидкость нужно помешивать с помощью кислотоустойчивой палочки.

При готовке электролита для щелочных аккумуляторов, нужно в руководстве по эксплуатации обязательно посмотреть рекомендуемое значение плотности.
В большинстве случаев плотность привязывается к +25°С – это позволит исключить вероятность замерзания и повреждения аккумулятора вследствие этого. Если же у вас температура отлична от этого показателя, то используя ареометр, вам своими руками нужно будет увеличить плотность. Это делается в пропорции 0.035 единиц на 5 градусов.
Соответственно, если температура ниже, то плотность понижается по такому же принципу.
Также обязательно для щелочных аккумуляторов нужно измерить изначальную плотность серной кислоты. В концентрированном варианте она равна 1.83 г/см3, если вы покупаете готовый электролит, то плотность 1.43 г/см3.
Процесс зарядки щелочного аккумулятора
Щелочные элементы питания с напряжением 12В заряжают как стандартными, так и альтернативными методами.
Стандартные режимы, рекомендованные производителями
Процесс в таком случае занимает не менее 12 часов. Аккумулятор заряжают в сухом отапливаемом помещении. Клеммы зарядного устройства подключают к токовыводам, после чего регулируют силу тока и напряжение. Допустимые параметры указываются на корпусе АКБ. Некоторые модели батарей поддерживают режимы ускоренной зарядки.
На первом этапе подают ток мощностью до 5 *С (С-номинальная емкость источника питания). Электролит прогревается, из-за чего процесс набора заряда ускоряется.
При быстрой зарядке нужно непрерывно отслеживать состояние аккумулятора. Ток высокой силы может перезарядить изделие и вывести его из строя.
Контроль осуществляют такими способами:
- С помощью светодиодов.На корпусах некоторых аккумуляторов расположены индикаторы, меняющие цвет в зависимости от уровня заряда. Второй светодиод отражает уровень напряжения. Такой способ контроля не является точным, т. к. индикаторы не всегда правильно реагируют на изменение параметров АКБ.
- Измерение напряжения.Этот параметр оценивают при наборе 80% заряда. До этого напряжение увеличивается медленно. Результат измерений может меняться в зависимости от температуры воздуха.
- Измерение баланса емкости.Вычислить показатель несложно. Трудности возникают при оценке коэффициента отдачи, который меняется в зависимости от силы выдаваемого ЗУ тока, состояния батареи и условий окружающей среды.
Замерить первоначальный уровень заряда получается не всегда. В таком случае время зарядки рассчитывают, беря за точку отсчета нулевой показатель.
Срок службы источника питания не учитывают. Если аккумулятор необслуживаемый, при зарядке измеряют давление электролита, напряжение на клеммах и температуру корпуса. Эти показатели во многом зависят от уровня заряда.
Компенсационный заряд
Существует 2 варианта компенсационной зарядки:
- Подача тока малой силы.На первом этапе выполняется стандартная зарядка. Через 10 часов силу снижают до 0,05 *С. Так батарея медленно заряжается, что препятствует саморазряду. Способ используется при отправке изделия на кратковременное хранение. Не рекомендуется пребывание элемента питания в таком состоянии более недели. Это негативно отражается на емкости АКБ. Правило не относится к никель-кадмиевым элементам.
- Резкое снижение силы тока.В течение первых 10 минут пускают 1 *С. По истечении этого времени параметр снижают в 10 раз. Зарядку продолжают в течение часа. Это помогает очистить пластины от сульфатного налета, насытить электролит кислородом и предотвратить миграцию кадмия. Не рекомендуется заряжать батарею этим методом в домашних условиях.
Нестационарные способы
В эту категорию входят методы, подразумевающие использование электроэнергии, параметры которой отличаются от заявленных в инструкции к АКБ. Подача переменного тока препятствует сульфатации пластин. В перерывах между импульсами наблюдается интенсивная выработка кислорода, ускоряющая процесс зарядки.
Характеристики электрической энергии остаются постоянными или меняются по мере набора заряда. Недостатком способа является невозможность применения для зарядки некоторых аккумуляторов, например AGM или гелевых.
Подготовка к процессу
Перед тем как начинать приготовление электролита, нужно подготовить все необходимые для этого вещи. Вам потребуются такие элементы процесса:
Специальная эбонитовая или керамическая посуда, объемом не менее 4 литров
Важно, чтобы посуда была стойкая к кислоте.
Инструмент для размешивания щелочных материалов. Так как делать это вы будете своими руками, то инструмент также должен тоже быть кислотоустойчивым.
Дистиллированная вода.
Ареометр.
Серная кислота
Обязательно требуется использовать специальную аккумуляторную серную кислоту.
Приготовление сопровождается соблюдением техники безопасности, вам потребуются:
- Резиновые перчатки.
- Халат или плотный фартук.
- Защитные очки для глаз.
- Нашатырная и борная кислота.
Только имея все необходимое, допускается своими руками готовить электролит.
Способ развести электролит для щелочного источника питания
Если электролит готовится под конкретную аккумуляторную батарею, то необходимо ознакомиться с сопутствующей инструкцией по эксплуатации, где будут указаны параметры плотности.
Если для приготовления раствора на щелочной основе используется твердая щелочь, то необходимо придерживаться следующих значений:
| Необходимая плотность раствора | Количество твёрдой щелочи равняется количеству электролита, разделенному на |
| 1,17–1,19 г/см³ | 5 |
| 1,19–1,21 г/см³ | 3 |
| 1,25–1,27 г/см³ | 2 |
Поэтапное приготовление:
- В тару вливается дистиллированная вода.
- Добавляется щелочь.
- Раствор смешивается до однородной полупрозрачной массы и выстаивается в закрытой таре не менее 5 часов.
- По истечении времени электролит считается готовым.